Séparer et combiner des substances
Réalise tes propres parures
...explore: La galvanisation
L’histoire de la galvanisation remonte au médecin "Luigi Galvani" qui découvrit ce phénomène le 6 novembre 1780.
Par galvanisation, nous comprenons tout le procédé durant lequel des métaux sont séparés éléctrochimiquement dans un liquide conducteur d’électricité (électrolyte) et transférés à d’autres objets métalliques. Le liquide conducteur d’électricité est une solution aqueuse du métal destiné à recouvrir l’objet. Dans notre expérience, nous dissolvons du sulfate de cuivre dans de l’eau pour cuivrer une plaquette en métal.
Pour cela, les pôles positifs et pôles négatifs sont plongés dans une solution de sulfate de cuivre et reliés à une source de tension constante (p.ex. une pile). Sous l'influence du courant électrique, les petites parties de cuivre (ion de cuivre) positives dans la solution sont libérées et se déplacent vers la plaque métallique au pôle négatif. Là, ils s'accrochent à la plaque en métal et la recouvrent d'un fine couche de cuivre.

1

Un revêtement mystérieux
A l'aide de produits chimiques et de courant, recouvre ta pièce métallique d'un mystérieux revêtement doré.

2
Matériel
Récipient avec sulfate de cuivre et acide citrique
3 piles de 1.5V
Aimants anneau, trombones
Rondelle de métal (laiton)
Raccords à pinces
Bâton en mousse rigide
Kit de lunettes, gants en latex
Une partie de la boîte en carton, fil plastique, papier blanc
Ruban adhésif, ciseaux, sac en plastique

3
Découpe les parties des lunettes de protection et assemble-les avec du ruban adhésif.

4
Modifie la longueur de la branche le long des lignes pointillées, de manière à ce que les lunettes tiennent bien.

5
Réalise avec une partie de la boîte en carton, un bassin de laboratoire. Utilise le sac en plastique pour protéger le reste du matériel.
Dépose un film plastique dans la boîte en carton et aplatis-le.

6
Couvre le fond de la boîte avec une feuille blanche.
Pose les lunettes et les gants à portée de main.

7
Prépare la solution
Mets les lunettes et les gants.
Ouvre le récipient avec le sulfate de cuivre et l'acide citrique dans le bassin de laboratoire.

8
Remplis le récipient aux deux tiers d'eau (flèche jaune).
Revisse le couvercle et secoue le récipient, jusqu'à ce que la poudre soit dissoute.
9
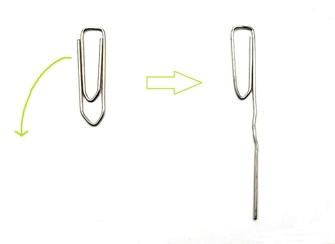
Plie le fil de fer vers l’extérieur et tends-le vers le bas (flèche verte).

10
Place le trombone comme sur l’image. La partie pliée vers le bas baigne dans la solution !
La solution de sulfate de cuivre a maintenant un aspect trouble et bleuâtre.

11
Assemblage de la source de tension de 4.5 Volt
- Pour la galvanisation au cuivre, nous avons besoin d’une source de tension de 4,5 Volt. Nous n’avons pourtant que des piles de 1,5 Volt. Que faire ? Qui trouve une solution?
- Coupe un morceau de 14 cm dans le bâton de mousse.

12
Relie les piles avec deux aimants anneaux. Pose deux autres aimants aux pôles libres. (flèches vertes)
Attention: Le pôle positif (+) d’une pile doit toujours être en contact avec le pôle négatif (-) de la pile voisine. (connexion en série).
Fixe les piles à la mousse avec de l’adhésif.

13
Préparation de la galvanisation
Connecte le pôle positif (+) de la source de tension au trombone sur le récipient.

14
Attention la pince doit bien tenir au trombone!

15

16

Galvanisation
Connecte la plaquette en métal au pôle négatif (-) de la source de tension.

17
Plonge entièrement la plaquette en métal dans la solution bleue de cuivre.
Aussitôt que la plaquette se trouve dans la solution, des bulles se créent sur le trombone ...

18
Attention!
La plaquette ne doit pas toucher le trombone.
La plaquette doit être constamment en mouvement et la solution doit être bien remuée.

19
Contrôle de temps en temps le changement de couleur de la plaquette.

20
Sors l’objet après environ une minute, rince-le avec de l’eau et sèche-le.
| Vues | |
|---|---|
| 30 | Total des vues |
| 30 | Vues Membres |
| 0 | Vues publiques |
Partager par email
S'il vous plaît S'identifier afin de partager ce webpage par email